
近期,“体检多年未检出癌症,患者确诊已是晚期转移” 的事件引发社会广泛关注。有患者连续多年体检均显示“正常”,却在近年被确诊为晚期癌症伴转移,令人痛心疾首。这一事件不仅关乎个体悲剧,更暴露了肿瘤早筛领域的深层问题:早筛为何未能及时发现风险?多早才算足够早?真正可靠的早筛方法应该是什么样的?今天,我们将从科学视角拆解这些核心问题,结合前沿技术进展,深入剖析这些问题的深层逻辑。
一、早筛“盲区”揭示肿瘤防治的时间紧迫性
在此类事件中,患者的体检报告连续多年未提示异常,但最终确诊时肿瘤已发生转移。这一矛盾背后反映了传统早筛方法的局限性:当肿瘤体积微小(直径<1厘米)或生物学行为特殊(如早期肾癌缺乏特异性标志物)时,常规筛查手段可能难以捕捉到风险信号。
癌症的发生发展是免疫系统与肿瘤细胞长期博弈的过程:
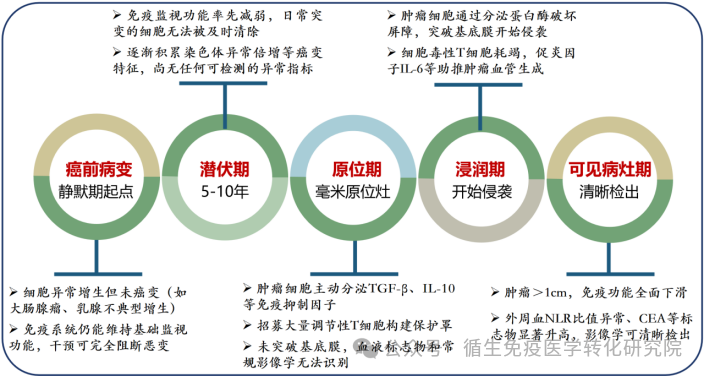
早筛的终极目标是在肿瘤仍可治愈或显著控制的阶段检出异常。若早筛能提前数月至数年预警风险,患者可能避免承受晚期治疗的痛苦与高昂成本。然而,此类事件中,传统手段未能穿透肿瘤的“静默保护期”,凸显早筛技术准确性与灵敏度的不足是致命短板。
二、多早算早?医学定义早筛的黄金干预窗口
肿瘤早筛的“早”并非简单以年龄或时间划线,而是严格依据生物学可干预阶段界定:(1)癌前病变与原位癌阶段(最理想):例如结直肠癌的腺瘤-癌序列需5~10年发展期,在此阶段通过肠镜切除腺瘤可100%阻断癌变。乳腺癌导管原位癌(0期)手术治愈率近100%。此阶段无症状,但筛查可精准拦截。(2)早期浸润癌阶段(次优但关键):肿瘤直径<3厘米且无转移(如Ⅰ期肺癌、肾癌),手术为主的治疗可获高生存率。早筛在此阶段介入,仍可显著降低死亡率。(3)微转移风险预警阶段:基于CTC/CTEC检测或ctDNA分析,在影像学可见病灶前数月至数年发现循环肿瘤信号,提示潜在转移风险,提前启动干预策略(如靶向治疗或密切监测)。世界卫生组织(WHO)及各国指南明确,有效的早筛必须满足两点:(1)检出的病变具备“干预后显著降低死亡率”的证据;(2)筛查结果可指导临床处理,且干预风险低于疾病进展风险。
三、常规早筛:为何年年体检仍漏诊?
漏检的悲剧不是孤例。在漏检事件的讨论中,许多人讲述着相似经历:甲状腺超声“正常”五个月后确诊癌症;母亲被告知“无问题”一个月后确诊晚期;公公在体检正常几天后诊断为白血病,不足一月离世。常规的检查手段仍然存在很多局限:

另一方面,当前多数体检中心采用“基础影像 + 标志物”的组合模式,看似全面实则存在系统性缺陷:(1)项目设计同质化:标准化套餐难覆盖个体风险差异(如吸烟人群缺LDCT筛查);(2)微小病灶检测阈值高:超声仅承诺检出≥1厘米肿块,而早期肾癌/肝癌常<1厘米时已具备转移潜能;(3)过度依赖单一指标解读;(4)价格≠准确性:高价套餐可能仅增重复项目(如多部位超声),未针对性补强核心技术(如液体活检),无法突破传统手段天花板;(5)常规手段仅满足解剖结构或生物标志物的单点检测,难以捕捉早期肿瘤的隐匿生物学行为(如循环播散或基因突变)。多年正常体检报告却最终晚期确诊的悲剧,正是这种局限性的缩影。
四、液体活检:突破传统瓶颈,重构肿瘤早筛的“时间维度”
当传统早筛手段困于“看得见(影像学)却不够早”“查得到(标志物)却不精准”的困境时,以血液为载体的液体活检技术正掀起一场早筛革命。这种无需穿刺或手术,仅通过外周血、尿液等体液即可捕捉肿瘤信号的技术,最大突破在于穿透肿瘤的“静默期”,在影像学可见病灶形成前数月甚至数年,就锁定其生物学异常。
液体活检的核心逻辑是“追踪肿瘤的‘分子足迹’”。肿瘤在生长过程中,会向血液释放两类关键信号:一是从原发灶或转移灶脱落的完整肿瘤细胞(CTC)及肿瘤血管内皮细胞(CTEC),二是肿瘤细胞坏死/凋亡释放的基因碎片(ctDNA)。通过精准捕获并分析这些信号,可实现“超早期预警 + 动态监测+ 精准溯源”的全周期管理,完美弥补传统手段的短板。
(一)循环肿瘤细胞(CTC)与循环肿瘤血管内皮细胞(CTEC) |
肿瘤转移的本质是“CTC定植”,原发灶癌细胞脱落进入血液,如同“种子”在远处器官生根发芽形成转移灶。而CTEC作为肿瘤新生血管脱落的内皮细胞,直接反映肿瘤的血管生成活性。对这两类细胞的检测,相当于在“种子”萌芽阶段就发现其踪迹。 应用优势:(1)全亚型捕获:传统方法依赖肿瘤表面标志物(如EpCAM),易漏检发生上皮-间质转化(EMT)的CTC(这类细胞转移能力更强)。而新一代技术(如SE-i・FISH®)通过“差相富集”技术,不依赖特定标志物,可捕获上皮型、间质型及混合型所有CTC/CTEC,避免“漏网之鱼”。(2)多维度分析:除了计数外,进一步通过荧光原位杂交(i・FISH)同步检测细胞的染色体倍体(异倍体提示恶性)、蛋白表型(如 HER2/PD-L1 表达指导用药)及器官特异性抗原(如肾癌的 PAX8、肝癌的 AFP),精准锁定肿瘤来源及转移风险。 临床价值:(1)超早期预警:当肿瘤仅数毫米(Ⅰ期甚至更早),影像学仍无显示时,CTC/CTEC已可被检出。研究证实,Ⅰ期肺癌患者CTC检出率达68%,比LDCT平均提前8个月发现风险。(2)转移风险分层:CTC计数≥2个/7.5mL血液的患者,复发风险是阴性者的3-5倍;CTEC阳性则提示肿瘤血管生成活跃,转移可能性更高。(3)疗效实时监测:治疗后CTC/CTEC数量下降,提示方案有效;若下降后回升,可能预示耐药或复发,比影像学早3-6个月发出预警。 |
(二)循环肿瘤DNA(ctDNA) |
ctDNA是肿瘤细胞释放到血液中的DNA片段,携带与原发灶一致的基因突变(如肺癌EGFR突变、结直肠癌KRAS突变)。通过测序分析这些突变,可在分子层面确认肿瘤存在。 应用优势:(1)高特异性:肿瘤特有的基因突变(如VHL突变之于肾癌)仅存在于ctDNA中,避免良性疾病干扰,假阳性率远低于传统标志物。(2)泛癌种筛查:通过多基因Panel检测,一管血可覆盖肺、肝、结直肠等多癌种,尤其适合无症状高危人群的广谱筛查。DECIPHER-RCC研究显示,基于ctDNA的肾癌早筛模型准确率达95%,可区分<25px早期肾癌与良性肾结节。(3)动态分子监测:ctDNA半衰期仅数小时,能实时反映肿瘤负荷变化。术后ctDNA持续阳性,提示残留病灶;治疗中突变丰度下降,说明疗效显著。 |
(三)多组学整合:1+1>2的精准协同 |
单一技术仍有局限(如ctDNA可能因肿瘤异质性出现假阴性,CTC检测受细胞稀有性影响),而“CTC/CTEC+ctDNA + 蛋白标志物”的多组学整合,可实现优势互补。例如,胃癌早筛中,ctDNA甲基化检测敏感性达82%,但特异性不足;联合CTC的EpCAM+CK + 表型分析后,特异性提升至94%,大幅降低误诊率。 |
五、肿瘤早筛:科学选择是关键
早筛的核心不是“越贵越好”,也不是“技术越新越好”,而是“适合自己的才是有效的”。结合自身风险、肿瘤类型和技术特点,科学选择筛查方案,才能真正实现“早发现、早干预”。
选择肿瘤早筛需结合自身风险分层:(1)普通人群可每年做基础筛查,选“超声(腹部/甲状腺/乳腺)+基础肿瘤标志物(CEA/AFP等)”,覆盖直径≥25px的实体瘤;(2)高危人群需针对性升级,比如长期吸烟者加低剂量螺旋CT(LDCT),胃肠癌高危者每2-5年做胃肠镜(或胶囊内镜),肝病患者加甲胎蛋白(AFP)+肝脏MRI。
新兴的液体活检技术(CTC/CTEC、ctDNA)更适合高危人群,有癌症家族史、慢性病或致癌暴露者可用CTC/CTEC超早期预警(比传统方法早6-12个月),术后患者动态监测防复发;想补全普筛未覆盖项目或评估多癌种风险,可选临床验证的ctDNA检测。
选筛查时别踩坑:不盲目追高端,PET-CT和“全项标志物”不适合健康人体检;优先选针对性套餐,比如肺癌高危人群配“LDCT+CTC”,避免重复检查;高危人群应把预算花在液体活检升级(如CTC分型)上,而非增加超声/CT的检查频次,这样才能精准高效地守住健康防线。
六、总结:精准早筛,守护生命起跑线
早筛漏检事件引发关注,让公众更聚焦肿瘤早筛的有效性与技术边界,揭开其“看似安全,实则滞后”的现实;早筛“黄金窗口”是可捕捉的生物学信号,传统影像、标志物困于“看得见却不够早”,而CTC/CTEC、ctDNA等液体活检正将早筛从“解剖可见”推向“分子可测”,为高危人群争得干预先机;选择早筛需“风险匹配”:普通人筑牢传统防线,高危人群用新技术补位以穿透“静默保护期”,唯有技术与个体风险深度结合,才能让“早发现、早干预”落地,对癌症而言,多一分精准便多一分改写命运的可能。









